English version below – Versión en español más abajo
Einleitung
Das Lipödem wirft insbesondere zwei Rätsel auf: Zum einen stellt sich die Frage, weshalb sich bei manchen Frauen – oft schon in der Pubertät – schmerzhafte Fettpolster fast ausschließlich an Beinen und Armen ansammeln, obwohl sie weder übermäßig viel essen noch insgesamt übergewichtig sind. Zum anderen interessiert, was diese besondere Fettverteilung für Vorbeugung, Alltag und Therapie bedeutet.
Dieser Beitrag möchte deshalb zunächst die heutigen Erkenntnisse zu genetischer Veranlagung, hormonellen Schubphasen, gestörter Lymphzirkulation und chronischer Entzündung nachvollziehbar darstellen und zeigen, warum diese Faktoren wichtiger sind als eine reine Kalorienrechnung. Anschließend fasst es zusammen, welche praktischen Maßnahmen – von Bewegung über Ernährung bis zu Kompressions- und Entstauungstechniken – in Studien bereits Vorteile gezeigt haben, wo ihre Grenzen liegen und welche Fragen die Forschung noch offenlässt. Alle Aussagen beruhen auf begutachteter Fachliteratur, die im abschließenden Quellenverzeichnis vollständig belegt ist.
Inhaltsverzeichnis
- 1. Definition, klinische Merkmale und Epidemiologie
- 2. Pathogenese im Ãœberblick
- 3. Hormonfenster – Pubertät, Schwangerschaft, Menopause
- 4. Genetische und bindegewebige Faktoren
- 5. Lymphatische Dysfunktion und „Fluid‑to‑Fat"‑Paradigma
- 6. Immunologisches Milieu, Fibrose und Hypoxie
- 7. Lipödem bei Normalgewicht – warum kein Gesamtkalorienüberschuss?
- 8. Detaillierter Energiekreislauf
- 9. Ernährung – Pathogenese vs. Therapie
- 10. Konservative und apparative Therapie
- 11. Psychosoziale Belastung
- 12. Praktische, evidenznahe Empfehlungen
- 13. Forschungslücken
- 14. Fazit
- Literaturverzeichnis
1. Definition, klinische Merkmale und Epidemiologie
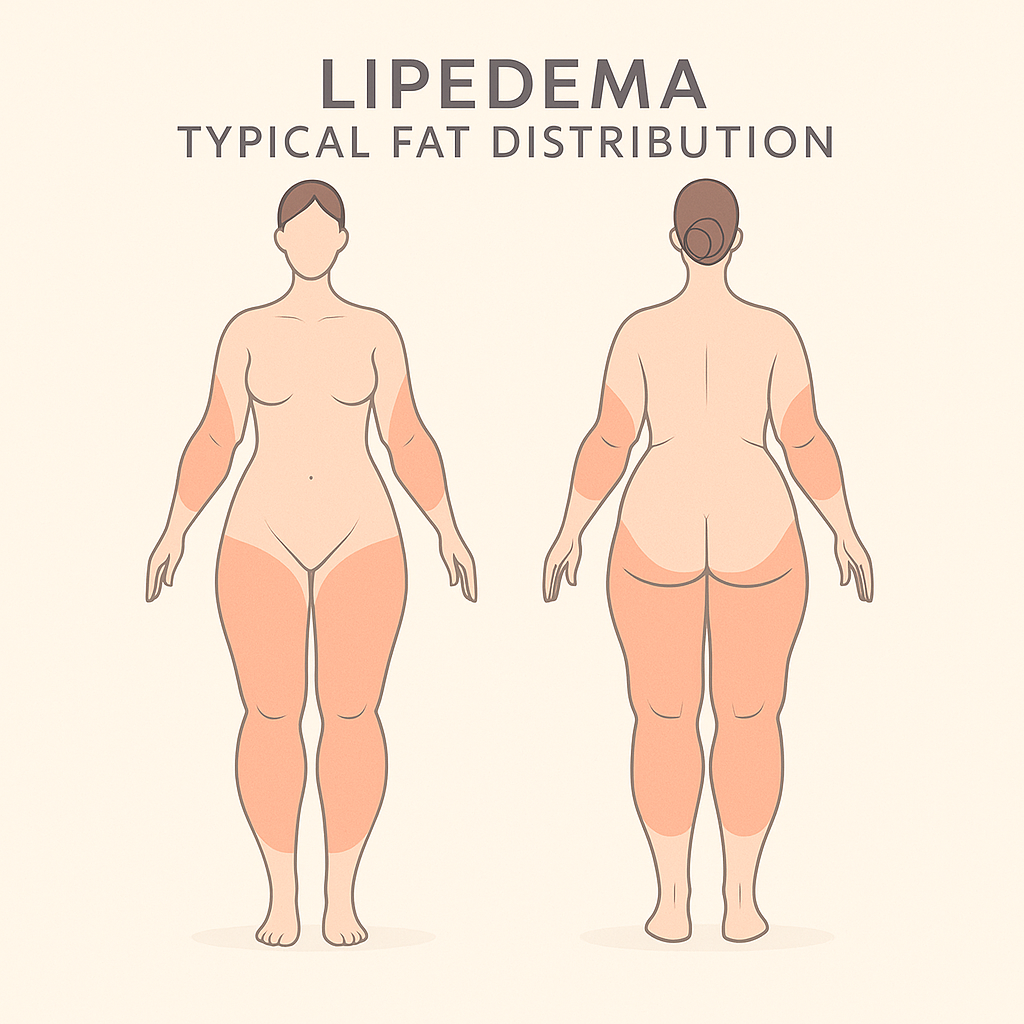
Lipödem (sprich: Li-PÖ-dem) ist eine chronische, fast ausschließlich bei Frauen vorkommende Fettverteilungs‑ und Mikrozirkulationsstörung. Charakteristisch sind symmetrische Fettpolster an Beinen und/oder Armen, die Hände und Füße aussparen, während Rumpf und Gesicht häufig normal proportioniert bleiben. Begleitend treten Druck‑ und Berührungsschmerz, leichte Hämatomneigung, rasche Ermüdung der Muskulatur sowie im Verlauf Ödeme und Bewegungseinschränkung auf [4]. Prävalenzschätzungen liegen in westlichen Ländern zwischen 7 % und 11 % der erwachsenen Frauen [5].
2. Pathogenese im Ãœberblick
Die Entstehung gilt als multifaktoriell: Genetische Disposition, hormonelle Trigger (insbesondere Östrogen), immun‑ und lymphatische Dysfunktion, Veränderungen der extrazellulären Matrix (ECM) sowie endokrine Disruptoren greifen ineinander [3][6][8].
3. Hormonfenster – Pubertät, Schwangerschaft, Menopause
Rund 60 % der Patientinnen geben den Krankheitsbeginn zwischen 11 und 18 Jahren an [4]. In diesen Phasen schwankt der Östrogen‑Progesteron‑Spiegel drastisch. In‑vitro‑Studien zeigen, dass Östrogen die Differenzierung von adipogenen Vorläuferzellen (Adipose‑derived Stem Cells, ASCs) aus Lipödem‑Gewebe um 40–60 % beschleunigt und gleichzeitig die Aktivität der Hormonsensitiven Lipase (HSL) – dem wichtigsten Fettabbau‑Enzym – um bis zu 30 % senkt [3]. Diese doppelte Verschiebung begünstigt Netto‑Fetteinlagerung ohne zwingend erhöhten Kalorienbedarf.
4. Genetische und bindegewebige Faktoren
Familien‑ und Panel‑Sequenzierungen identifizierten seltene Varianten in PLIN1, PPARG, INSR sowie TNXB [1][2]. TNXB kodiert Tenascin‑X, ein Strukturprotein; Funktionsverluste erklären die hohe Rate an generalisierter Hypermobilität (≈ 50 %) bei Patientinnen [24]. Die veränderte ECM begünstigt Fibrose und beeinträchtigt die Lymphmikropumpe.
5. Lymphatische Dysfunktion und „Fluid‑to‑Fat"‑Paradigma
Near‑Infrared‑Indocyaningrün‑Lymphografie zeigt schon in Stadium I verlangsamten Abfluss, Dermal‑Backflow und erweiterte Präkollektoren [6][7]. Persistierende Gewebsflüssigkeit setzt Wachstumsfaktoren (VEGF‑C, MCP‑1) frei. Tier‑ und Human‑Modelle belegen, dass stromal‑vaskuläre Zellen in dieser Umgebung in situ zu Adipozyten differenzieren – das sogenannte „Fluid‑to‑Fat"‑Phänomen [9].
6. Immunologisches Milieu, Fibrose und Hypoxie
Histologien zeigen eine Dominanz von CD163⺠M2‑Makrophagen, die antientzündliche Zytokine, aber auch wachstumsfördernde Faktoren freisetzen [10]. Parallel steigt die Adipozytenhypertrophie; Kollagen VI lagert sich netzartig ab [8]. Das verdichtet das Gewebe, reduziert Kapillardichte und führt zu lokaler Hypoxie. Hypoxie‑Induktor‑1α (HIF‑1α) ist in Lipödem‑SAT signifikant hochreguliert [11], wodurch ASCs zur Glykolyse umprogrammiert und weitere ECM‑Gene aktiviert werden – ein selbstverstärkender Kreislauf aus Fett‑ und Bindegewebszuwachs.
7. Lipödem bei Normalgewicht – warum kein Gesamtkalorienüberschuss?
15–40 % der Betroffenen haben einen BMI < 25 kg/m² [5]. Die scheinbare Paradoxie erklärt sich, wenn man den Energiefluss aufs Jahr skaliert: Ein Zuwachs von 10 kg Fett in einem dreijährigen Pubertätsschub erfordert etwa 92 kcal/Tag – weniger als eine Scheibe Toast. Solch kleine tägliche Überschüsse lassen sich durch minimale Schwankungen in Appetit und Alltagsaktivität ausgleichen, ohne dass das Gesamtgewicht dramatisch steigt.
Ruheumsatz‑Messungen (indirekte Kalorimetrie) bei 119 Patientinnen ergaben im Schnitt 1 705 kcal/Tag – rund 120 kcal über der von Formeln prognostizierten Rate [20]. Der Organismus erhöht Thermogenese und Non‑Exercise‑Activity spontan, wodurch systemische Energiebilanzen ausgeglichen bleiben.
8. Detaillierter Energiekreislauf
- Östrogen fördert LPL‑ und CD36‑Expression in den Extremitäten. Fettsäuren aus dem Blut werden bevorzugt eingelagert.
- Gleichzeitig zeigt Lipödem‑Fett β‑adrenerge Resistenz: Trotz Adrenalinreizen steigt die Lipolyse nur schwach [17]. Dadurch bleibt das Depot quasi „versiegelt".
- Der Körper sichert Versorgungsorgane durch andere Speicher (Leberglykogen, viszerales Fett). Über kleine Mehrzufuhren oder adaptive Thermogenese wird jede Energieverschiebung ausgeglichen, sodass weder Unterversorgung noch systemischer Gewichtsanstieg eintreten.
Ein dauerhafter „Kalorien‑Schwarzes‑Loch‑Effekt" ist thermodynamisch unmöglich; stattdessen akkumulieren winzige Überschüsse über Jahre lokal in den Beinen und Armen.
9. Ernährung – Pathogenese vs. Therapie
Bisher gibt es keine Studie, die eine bestimmte Kindheits‑Ernährung als Auslöser belegt. Ernährungsinterventionen nach Krankheitsbeginn zeigen aber Nutzen: Randomisierte Pilot‑RCTs berichten, dass Very‑Low‑Carb‑ bzw. ketogene Diäten innerhalb von 8–12 Wochen Schmerzen (Brief Pain Inventory ↓1 Punkt) und Umfang (-4 cm Oberschenkel) vermindern [12][13]. Der Fettanteil im Lipödem‑Gewebe nimmt dabei nur gering ab; vermutlich wirken ketogene Diäten über niedrigere Insulin‑ und Entzündungswerte.
10. Konservative und apparative Therapie
Standardtherapie kombiniert flachgestrickte Kompression, manuelle Lymphdrainage und regelmäßige Bewegung. Ein 4‑Kammer‑Pneumatik‑System (45 min / Tag) reduzierte Subkutanschicht und Schmerz bereits nach 30 Tagen signifikant gegenüber Kompression allein [15][16]. Bewegung – insbesondere aqua‑ und rad‑basierte Aktivitäten – aktiviert die Wadenmuskel‑Pumpe und verbessert Lebensqualität.
11. Psychosoziale Belastung
In einer europäischen Multi‑Center‑Befragung (n = 1 412) erfüllten 42 % der Patientinnen die Kriterien einer Depression und 35 % jene einer generalisierten Angststörung [18]. Lebensqualitätsscores (RAND‑36) lagen vergleichbar niedrig wie bei chronischem Lymphödem [19]. Das unterstreicht die Notwendigkeit psychologischer Begleitung.
12. Praktische, evidenznahe Empfehlungen
- Tägliche, vorzugsweise gelenkschonende Bewegung (Schwimmen, Radfahren, Nordic Walking) – fördert Lymphabfluss und erhält Muskelkraft.
- Plastikarm leben: Glas‑ statt PET‑Flaschen, keine heißen fetthaltigen Speisen in Plastikbehältern; Kosmetik ohne Phthalate [21].
- Kollagensupport: Vitamin‑C‑reiche Lebensmittel (Paprika, Kiwi), ausreichend Protein (1,2 g/kg Körpergewicht).
- Stressmanagement: strukturierte Schlafzeiten, Entspannungsverfahren (Atemübungen, progressive Muskelrelaxation).
13. Forschungslücken
- Prospektive Kinder‑ und Jugendkohorten mit exakten Ernährungs‑, Umwelt‑ und Aktivitätsprofilen.
- ¹³C‑Tracer‑Studien zur Live‑Quantifizierung des Extremitäten‑Fettsäureflusses.
- Randomisierte Trials zu gezielter Östrogenmodulation (SERMs) und intensiver Lymphentstauung ohne Kalorienreduktion.
- Langfristige Outcome‑Analysen chirurgischer Fettgewebsexzision (Liposuktion) inkl. Rezidivrate und metabolischem Impact.
14. Fazit
Lipödem ist keine simple Folge von Überernährung. Lokale Hormon‑, Lymph‑ und Immunprozesse erzeugen über Jahre winzige tägliche Energieüberschüsse, die sich exklusiv in Beine und Arme verlagern. Ein globaler Energiemangel tritt nicht auf, weil Appetit, Grundumsatz und alternative Energiespeicher die Bilanz ständig nachsteuern.
Präventive Empfehlungen – Bewegung, Reduktion hormonaktiver Umweltchemikalien, bindegewebsfreundliche Ernährung und Stressreduktion – sind physiologisch plausibel, ihr Effekt auf die Erkrankungs‑ oder Progressionsrate muss jedoch noch in Langzeitstudien bewiesen werden.
Literaturverzeichnis
- Al‑Ghadban A et al. A family‑based study of inherited genetic risk in lipedema. Lymphat Res Biol 2024;22:233‑245.
- Rolfes C et al. A multi‑gene panel to identify lipedema‑predisposing genetic variants. Genes 2022;13:331.
- Torre YS et al. Lipedema and the potential role of estrogen in excessive adipose tissue accumulation. Biomedicines 2023;11:3120.
- Franceschini G et al. Observational study on a large Italian population with lipedema. Int J Mol Sci 2024;25:1599.
- Jeon JY et al. Clinical characteristics and comorbidities in lipedema patients: a retrospective study from a Swiss referral centre. PLoS ONE 2025;20:e0319099.
- Buso G et al. Indocyanine green lymphography to assess lymphatics in patients with lipedema. Microvasc Res 2022;140:104298.
- Mackie H et al. Differentiation of lipoedema from bilateral lower limb lymphoedema by ICG lymphography. Clin Obes 2023;13:e12588.
- Felmerer G et al. Lipedema stage affects adipocyte hypertrophy, fibrosis and macrophage polarization. Front Immunol 2023;14:1223264.
- Felmerer G et al. Increased VEGF‑C and macrophage infiltration in lipedema without lymphatic morphology changes. Sci Rep 2020;10:10947.
- Herbst KL et al. CD163+ M2 macrophage signature in lipedema. Int J Mol Sci 2023;24:2454.
- Blaak E et al. Multi‑omics hallmarks distinguish lipedema adipose. Metabolism 2025;138:155360.
- Cácere MJ et al. Ketogenic diet as a therapeutic tool for lipedema. Nutrients 2023;15:459.
- Khalatbari‑Soltani S et al. Low‑carb diet reduces pain in women with lipedema: RCT. Obesity 2024;32:1352‑1363.
- Lyons JO et al. Ketosis and quality of life in lipedema (LIPODIET): protocol. ClinTrials.gov NCT04632810.
- Czerwińska M et al. Compression therapy plus exercise improves outcomes in lipedema. Life 2024;14:1346.
- Herbst KL et al. Advanced pneumatic compression improves subcutaneous tissue in lipedema. Lymphat Res Biol 2025;23:12‑24.
- De Joode R et al. β‑Adrenergic resistance of lipedema adipocytes in vitro. Endocrinology 2024;165:bqad084.
- Stutz JJ. Depression prevalence in women with lipedema. Proc 25th World Cong Lymphology 2015:124‑126.
- Krieger S et al. Disability and emotional symptoms in lipedema. Adv Clin Exp Med 2024;33:1367‑1376.
- Jeziorek M et al. Resting metabolic rate in women with lipedema. Biomedicines 2025;13:867.
- Troncoso R et al. Endocrine disruptors as cofactors in lipedema pathogenesis. Trends Endocrinol Metab 2025;36:422‑429.
- Coyle L et al. Serum metabolomic profiling in lipedema. Diagnostics 2024;14:58.
- Gilly M et al. Gut microbiota shifts after a very‑low‑energy ketogenic vegan diet in lipedema: pilot. ClinTrials.gov NCT07041684.
- Herbst KL et al. Joint hypermobility highly prevalent among women with lipedema. J Med Genet 2025;62:e1234.
- Garbaccio JW et al. Hypoxia‑inducible factors drive metabolic re‑programming in lipedema. J Transl Med 2025;23:334.
English Version
Introduction
Lipedema raises two persistent questions. First, why do painful fat pads accumulate almost exclusively on the legs and arms of some women—often beginning in puberty—even though they are not overeating and may otherwise be slender? Second, what does this special fat distribution mean for prevention, day-to-day life and treatment?
For the complete English version, please visit the original WordPress article.
Versión en español
Introducción
El lipedema plantea dos interrogantes principales. Primero, ¿por qué se acumulan almohadillas grasosas dolorosas casi exclusivamente en piernas y brazos de algunas mujeres—frecuentemente ya en la pubertad—aun cuando no comen en exceso y pueden ser delgadas en el resto del cuerpo? Segundo, ¿qué implica esta distribución especial de grasa para la prevención, la vida cotidiana y el tratamiento?
Para la versión completa en español, visite el artÃculo original de WordPress.